記事・インタビュー

はじめに
輸液の3Rのうち、前回からはRedistributionである補正を取り扱いました。特にあえて無視されがちな酸塩基平衡である代謝性アルカローシスを扱いました。今回も同じくRedistributionで、代謝性アルカローシスに次いで頻度の高い、代謝性アシドーシスを扱います。特に比較的悩みやすいであろうポイント、反射的になんとなくやってしまいがちなポイントについて、皆さんと学びを深めたいと考えています。
テーマ予定
シリーズ1. 輸液の適応を3Rで整理する
シリーズ2. 救急外来でのリアルワールド輸液を再考する:Non criticalとCriticalに分類
シリーズ3. Resuscitation:Criticalな患者の輸液総論~“ROSD” 敗血症を例に~
シリーズ4. Resuscitation:敗血症のOptimization phaseをどう乗り切るか?~特に侵襲的モニタリングなし~
シリーズ5. Resuscitation:敗血症のStabilizationやDe-escalation phaseをどうするか?
シリーズ6. Redistribution:あえて代謝性アルカローシスを例に考える
シリーズ7. Redistribution:代謝性アシドーシスを例に考える※今回
シリーズ8. Redistribution:低K血症の補正
シリーズ9. Routine maintenance:Non criticalの急性期維持輸液
シリーズ10. Redistribution:低Na血症の補正を超深掘り
Redistribution:代謝性アシドーシスを例に考える
1)代謝性アシドーシスも重症患者を中心に頻度が高く、死亡率にも影響する
2)乳酸アシドーシスをみて、なんとなく輸液はご法度!pCO2ギャップやRERsurを使ってType AかType Bの乳酸アシドーシスか鑑別し、対応も使い分けよう
頻度・死亡率の観点で代謝性アシドーシスを考えてみよう
(無視されることが多い)代謝性アルカローシス以上に、実臨床で頭を悩ませがちなのが代謝性アシドーシスです。きっと読者の皆さんもそのようにお感じでしょう。実際、日本と台湾のICUの観察研究で、ICU患者のなんと14%に中等度以上の代謝性アシドーシスが生じていたという報告があります 1)。頻度が高いだけではありません。pH<7.3の代謝性アシドーシスをもつICU患者は、ICU死亡率が17.3% 2)、pH<7.2の重度の代謝性アシドーシスで、SOFAスコア4点以上であれば、ICU死亡率が43.5%というデータすらあります 3)。頻度・死亡率の2つの観点からも、代謝性アシドーシスは極めて臨床的に重要だといえるでしょう。代謝性アルカローシスと並んで、酸塩基平衡の双璧と筆者は考えています。
そんな代謝性アシドーシスですが、その内訳を考えてみましょう。臨床でよく出合う代謝性アシドーシスは、糖尿病性ケトアシドーシス(Diabetic ketoacidosis:DKA)、乳酸アシドーシス、AG非開大性代謝性アシドーシス(以下、Non-gap acidosisと称します)とされています。
その中で、DKAは治療方針がガイドライン・総説でかなりかっちり提唱されているので、診断さえついてしまえば、悩むことは少ないように個人的には感じます。むしろ、乳酸アシドーシスやNon-gap acidosisにこそ、悩みが隠れているのではないでしょうか? 実際、「乳酸上昇をみたら、ひとまず輸液して乳酸を希釈させる、乳酸をウォッシュアウトさせる」という根拠があいまいな “なんとなく輸液:fluid reflex”という診療を時にみかけます。“なんとなく輸液:fluid reflex”から脱却するためにも、今回は、乳酸アシドーシスにフォーカスしてみましょう。
乳酸の産生と代謝を俯瞰してみよう
乳酸は動脈血液ガスで簡便に測定できるため、皆さんにとってもなじみのあるものだと思いますが、その産生や代謝機序は意外とイメージが湧きづらいかもしれません。図を使いながら生化学を復習してみましょう(図1)。
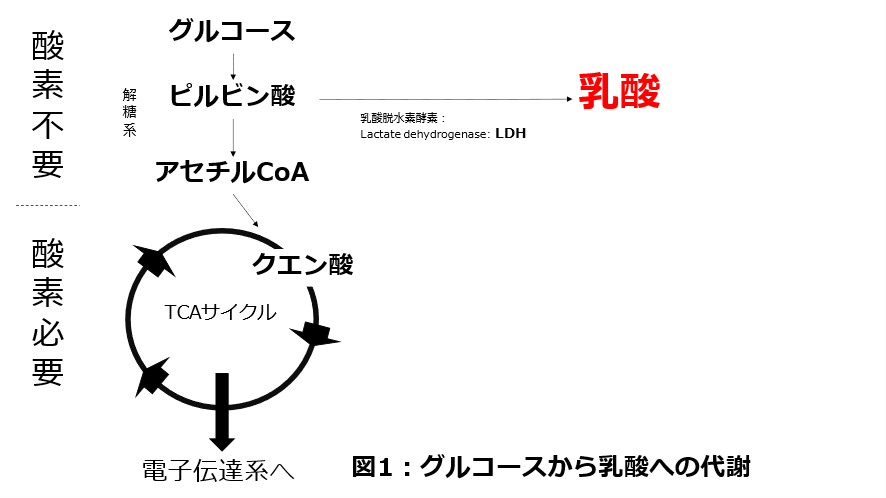
細胞はエネルギー産生をするためにグルコースを解糖系でピルビン酸にします。その後、ピルビン酸からアセチルCoAに代謝し、TCAサイクル・電子伝達系を介して大量のATPを産生します。特にTCAサイクルから電子伝達系は酸素を必要としながら行う代謝、好気性代謝でした。
つまり、酸素を消費しながら効率よく大量のエネルギーを産生するシステムです。一方で、十分に酸素が届かないと細胞は別の反応を起こします。具体的にはピルビン酸から乳酸脱水素酵素(Lactate dehydrogenase: LDH)の力を借りて、乳酸を産生、ここからATPの産生量は少ないながらもエネルギーを作りだす嫌気性代謝をします。
このグルコースから乳酸を作るシステムはほぼすべての細胞に備わっています。なお、話が脱線しますが、生化学検査の検査項目であるLDHは様々な臓器障害で上昇します。これはほぼすべての細胞で乳酸を産生するシステムをもっている、その酵素である乳酸脱水素酵素:LDHをもっているからこそだと理解できれば、納得できますね。
この乳酸は、ほぼすべての細胞が産生できることもあってか、産生量は平常時でだいたい0.9~1mmol/kg/hとされており、体重が60kgだとだいたい1日1200mmolの大量の乳酸を産生しているといわれています。この量は驚きではありませんか?「え?でも、平常時は乳酸って上昇していないと思うけど?」とお感じになった読者の方もいらっしゃるでしょう。大変鋭いです。これだけ大量の乳酸を平常時で産生しているのにもかかわらず、血液中の乳酸値が低く抑えられているのは、乳酸の代謝、クリアランスの能力が極めて高いからです。乳酸クリアランスは幅がありますが、0.7~7.2mmol/L/h程度とされています 4)。ちょっとした乳酸であれば数分でクリアランスできるほどの能力です。逆に言えば、血液中で乳酸値が上昇していれば、このクリアランス以上に大量の乳酸が産生されている状態で、細胞の代謝が異常事態、緊急事態ということが納得できるかと思います。
乳酸アシドーシスを分類する
乳酸値が上昇し、代謝性アシドーシスになっている状態は細胞の代謝がおかしい、緊急事態だということをご理解いただいた上で、では、リアルワールドで、乳酸アシドーシスに出合ったらどう動いたらよいでしょうか? 先ほどの図1を思い出してみましょう。

原理的に考えれば、酸素を使っての好気性代謝がなんらかの理由でうまくいっていない、または作られた乳酸のクリアランスが落ちている原因を考えればよさそうです。これを元に実臨床では、酸素が細胞に届かずに生じ、組織で乳酸産生が亢進している組織低酸素・低還流の機序での乳酸アシドーシスをType A、それ以外をType Bとして鑑別をしていくことをKrautらは提唱しています 5)(表1)。

具体的にみていきましょう。このType Aの乳酸アシドーシスは細胞へ酸素が届けられていない、言い換えれば、酸素運搬量:DO2(Oxygen delivery)が低下した状態です。DO2は心拍出量:CO(Cardiac output)と動脈血酸素含量:ACtO2(O2 content)を用いて以下の式で表せることが知られています。
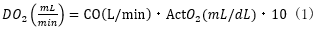 *10をかけるのは/dLを/Lの補正のため
*10をかけるのは/dLを/Lの補正のため
また、動脈血酸素含量:ACtO2 は以下の式で表せることが知られています。
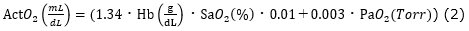
この(1)(2)の式を組み合わせると、以下のことがわかります。
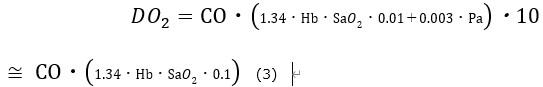
つまり、Type Aの乳酸アシドーシスは、主に、心拍出量の低下、Hbの低下、ひどいSaO2≒SpO2の低下で生じるといえます。表1の鑑別と一致しますね。実際には、さらにこのような全身のDO2低下だけでなく、局所のDO2低下≒局所の虚血や、酸素需要の増加(需要の割には相対的に酸素を運搬できていないもの)も含めてType Aアシドーシスとしています。
では、理屈がわかってきたところで、「これはType Aの乳酸アシドーシス」とベッドサイドで判断するにはどうしたらよいでしょうか? お気づきの通り、Type Aの乳酸アシドーシスといっても、様々な原因があります。大事なポイントはType Aの乳酸アシドーシスかどうかの判断を平均動脈圧だけで判断しないです。ショックを血圧だけで判断しないということと同様ですね。「じゃあ、どうするの?」という声が聞こえてきました。大丈夫です。この記事では、ベッドサイドで実際に使えるポイントをお伝えします。是非、乳酸アシドーシスをみたら、動脈からの血液ガスと中心静脈からの血液ガス(CVから逆血させて採取)をとり、pCO2ギャップ、RERsurを計算、時にScvO2と組み合わせて判断してください 6)。
中心静脈での血液ガスで自信がつく①!
「なんかよくわからない用語が出てきた…」と慌てることなかれ!さらに説明していきます。結論からいうと、の動脈からの血液ガスと中心静脈からの血液ガスの組み合わせは乳酸アシドーシスの鑑別で極めて重要な役割を果たします。心拍出量:COは、Fickの原理を用いて、CO2関連のパラメーターを使って表せることが知られています。特にCO2産生量(VCO2)と動脈血液中のCO2含量(ACtCO2)と静脈血液中のCO2含量(VCtCO2)を用いると、以下の関係が知られています。
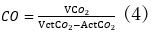
このCO2含量の静脈と動脈での差:VCtCO2-ACtCO2は、CO2分圧を用いて別の表現ができます。具体的には静脈と動脈でのCO2含量の差は、静脈と動脈でのCO2分圧の差に比例するので、
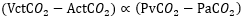
係数:kを用いることで、
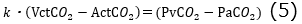
この(4)(5)の式を組み合わせることで、以下の式となります。
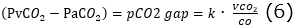
この静脈(正確には中心静脈)と動脈でのCO2分圧の差:(PVCO2-PaCO2)は、pCO2ギャップと呼ばれます。この(6)式からおわかりの通り、pCO2ギャップは心拍出量:COと反比例します。もう少し砕けた表現をすれば、「COが低下すれば、pCO2ギャップが上昇する」「pCO2ギャップが上昇していれば、COの低下があるかも」と疑えるというわけです。
このpCO2ギャップは優れた指標で、実は大きな循環であるCOと関係がある以外に、COが低下していなくても微小循環が悪い場合にも上昇することが知られています。そのため、pCO2ギャップはCOにとどまらず、還流全体を表す指標と言った方がより正確かもしれません。なお、このpCO2ギャップは敗血症を中心に研究が進められていますが、Waldaufらは敗血症以外でも使える可能性を、ケースシリーズを通して示唆しています(6)。筆者も敗血症に限らず乳酸アシドーシス全般でpCO2ギャップは使用しています。このpCO2ギャップのカットオフ値は、敗血症の場合は6Torr(0.8kPa)と知られており、pCO2ギャップが6以上であれば、ギャップありと判断します(7)。一方、敗血症以外でのpCO2ギャップの明確なカットオフ値は確立されていませんが、先述のWaldaufらの提案に基づき、3.7Torr(0.5kPa)以下であれば、明確にギャップなしと判断し、7.5Torr(1.0kPa)以上であれば明確にギャップありと筆者は判断しています(6)。なお、敗血症以外のケースで、3.7~7.5Torrのグレーゾーンになった場合は、ほかの指標と合わせて判断し、それでも悩ましい場合はType AとType Bの乳酸アシドーシスの鑑別を両方するように筆者はしています。
上記のようなグレーゾーンが存在しうるほか、pCO2ギャップも注意しなければいけない点が当然あります。どんな指標もピットフォール、偽陽性があるからです。具体的には、pCO2ギャップは高体温、重度の代謝性アシドーシス、Hbの著しい上昇の状況下では、還流の異常がなくてもギャップありになってしまうことが知られています。そのため、筆者は、先述のWaldaufらの提案に基づき、さらにもう1つの中心静脈での血液ガスも用いた指標:RERsurを組み合わせています。
中心静脈での血液ガスで自信がつく②!
組織の代謝は酸素消費量に対して、CO2をどれくらい産生するかという、Respiratory exchange ratio: RER(これは呼吸商とほぼ同義と思ってください)の影響を受けます。糖を用いてエネルギーを産生する場合、酸素1 molに対してCO21 molを産生、脂質なら0.7 mol、アミノ酸なら0.84 molということが知られています。さらに、嫌気性代謝になるとこのRERは1.0を超えることが知られています。この組織内でのRERは直接計算しづらいので、Waldaufらは動脈と中心静脈のデータを用いた代替的なものとして、RERsurを提案しています(6)。
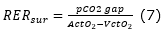
なお、ACtO2は先述の動脈血酸素含量、VCtO2は中心静脈血酸素含量で、それぞれ以下の式で表せます。
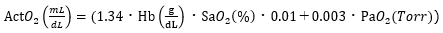
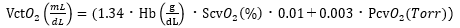
このRERsurは、pCO2ギャップの単位がTorr、ACtO2やVCtO2の単位がmL/dL場合、カットオフ値が1.4であることが知られています(8)。つまり、RERsur>1.4であれば、組織低酸素だと判断できるというわけです。なお、このRERsurもピットフォールはあり、敗血症や肝硬変、血液透析患者など末梢でシャントが生じる疾患では値が上昇することが知られています。
中心静脈での血液ガスで自信がつく③!
最後に、循環の大事な指標であるScvO2にもここで触れたいと思います。まずは図2をご覧ください。
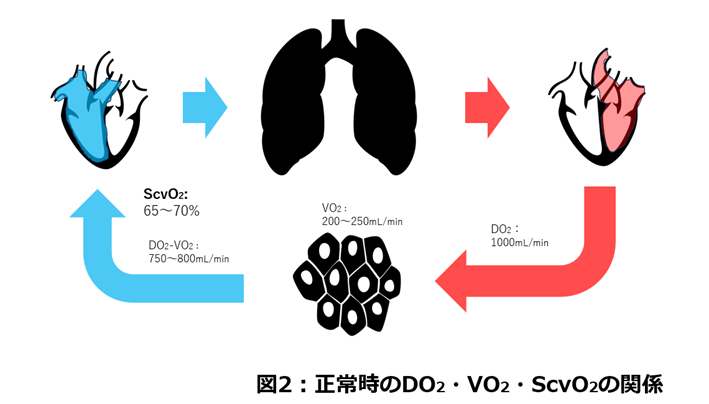
肺で十分に酸素化された動脈血は、末梢の細胞に酸素を届けます。この末梢の細胞で消費される酸素摂取量VO2は200~250mL/min程度であることが知られています。酸素が消費された静脈血は心臓に戻り、また肺で酸素化されて…という循環をしていきます。図2をみておわかりの通り、静脈血、特に中心静脈血の酸素飽和度ScvO2はDO2-VO2と正の相関があります。DO2は組織低酸素・低還流の中心的な指標であることは先述の通りです。つまり、ScvO2も乳酸アシドーシスの鑑別の際には重要な項目の1つです。具体的には、ScvO2が65~70%を下回っていれば、DO2の低下、またはVO2の上昇(で相対的にDO2が足りていない)を疑います。なお、組織低酸素・低還流があってもScvO2が基準値内(偽陰性)になってしまうピットフォールも同時に押さえておきましょう。具体的には敗血症などの酸素利用障害、肝硬変や血液透析患者などの末梢でのシャントがある場合、微小循環が悪い場合などです。
では、今までのpCO2ギャップ、RERsur、ScvO2を使って乳酸アシドーシスの鑑別をしてみましょう。これらの指標の中で、pCO2ギャップは組織低酸素・低還流をより感度よく見つけられるとWaldaufらは提唱します 6)。このWaldaufらの意見と、Andersenらの提案する乳酸上昇時のアプローチ 9)を合わせて、筆者は以下のように乳酸上昇・乳酸アシドーシスの時の鑑別を進めています(表2)。

なお、Step②でも記載していますが、微小循環障害については、2023年現在、積極的に見つけて輸液やカテコラミンの介入をしても予後を変えなさそう 10)といわれています。そのため、筆者は乳酸アシドーシスの原因がType Aに分類されるも、CO・SaO2・Hbが問題なく、局所循環で四肢の虚血や非閉塞性腸間膜虚血(Non-occlusive mesenteric ischemia: NOMI)など致死的なものが除外されれば、微小循環障害かもとして、ただ輸血やカテコラミンなどの介入をしても予後を変えないため、無理に輸液などはせずに慎重に経過をみるスタンスをとっています。
終わりに
最後にまとめとして、乳酸アシドーシスのイメージ図を掲載します(図3)。

以上、代謝性アシドーシス、特に乳酸アシドーシスの話を中心にお伝えしてきました。乳酸アシドーシスの原因の性質上、輸液の3RのうちのRedistributionだけでなく、Resuscitationの要素も大きい内容になってしまいましたが、いかがだったでしょうか?もし、ちょっとよくわからないということがあれば、過去の連載のResuscitationの所も読み直していただくと理解が深まるかもしれません。
さて、次回はRedistributionの王道の1つ、低K血症を扱います。お楽しみに!
<参考文献>
1)Fujii T, Udy AA, Nichol A, Bellomo R, Deane AM, El-Khawas K, et al. Incidence and management of metabolic acidosis with sodium bicarbonate in the ICU: An international observational study. Crit Care. 2021 Feb;25(1):45.
2)Mochizuki K, Fujii T, Paul E, Anstey M, Pilcher DV, Bellomo R. Early metabolic acidosis in critically ill patients: a binational multicentre study. Critical Care and Resuscitation. 2021 Mar ;23:67–75.
3)Jaber S, Paugam C, Futier E, Lefrant JY, Lasocki S, Lescot T, et al. Sodium bicarbonate therapy for patients with severe metabolic acidaemia in the intensive care unit (BICAR-ICU): a multicentre, open-label, randomised controlled, phase 3 trial. Lancet. 2018 Jul;392(10141):31–40.
4)Dezman ZDW, Comer AC, Smith GS, Hu PF, Mackenzie CF, Scalea TM, et al. Repeat lactate level predicts mortality better than rate of clearance. Am J Emerg Med. 2018 Nov;36(11):2005–9.
5)Kraut JA, Madias NE. Lactic acidosis. N Engl J Med. 2014 Dec;371(24):2309–19.
6)Waldauf P, Jiroutkova K, Duska F. Using pCO2 Gap in the Differential Diagnosis of Hyperlactatemia Outside the Context of Sepsis: A Physiological Review and Case Series. Crit Care Res Pract. 2019 Dec;2019:5364503.
7)Vallée F, Vallet B, Mathe O, Parraguette J, Mari A, Silva S, et al. Central venous-to-arterial carbon dioxide difference: an additional target for goal-directed therapy in septic shock? Intensive Care Med. 2008 Dec;34(12):2218–25.
8)Mekontso-Dessap A, Castelain V, Anguel N, Bahloul M, Schauvliege F, Richard C, et al. Combination of venoarterial PCO2 difference with arteriovenous O2 content difference to detect anaerobic metabolism in patients. Intensive Care Med. 2002 Mar;28(3):272–7.
9)Andersen LW, Mackenhauer J, Roberts JC, Berg KM, Cocchi MN, Donnino MW. Etiology and therapeutic approach to elevated lactate levels. Mayo Clin Proc. 2013 Oct;88(10):1127–40.
10)Bruno RR, Wollborn J, Fengler K, Flick M, Wunder C, Allgäuer S, et al. Direct assessment of microcirculation in shock: a randomized-controlled multicenter study. Intensive Care Med. 2023 Jun ;49(6):645–55.
<プロフィール>

柴﨑 俊一(しばざき・しゅんいち)
ひたちなか総合病院 総合内科
2010年、筑波大学医学専門学群医学類を卒業。諏訪中央病院にて初期研修を経て、2012年に同病院内科研修医。
その後、名古屋第二赤十字病院腎臓内科にて国内留学、諏訪中央病院にて腎臓・糖尿病内科/総合内科として勤務後に2017年から現職。
個人としては”日本の墨子”を目指し、組織としては、茨城1愛ある診療を目標にかかげる。市中病院改革:特に教育改革、ボトムアップ型組織マネジメントを進めている。
柴﨑 俊一
このシリーズの記事一覧
-
記事

3Rで整理する 輸液の基本の「き」 ~輸液の適応を3Rで整理する~
- 研修医
- 専攻医・専門医
3Rで整理する 輸液の基本の「き」 ~輸液の適応を3Rで整理する~
柴﨑 俊一
-
記事

3Rで整理する 輸液の基本の「き」 ~救急外来でのリアルワールド輸液を再考する:Non criticalとCriticalに場合分け~
- 研修医
- 専攻医・専門医
3Rで整理する 輸液の基本の「き」 ~救急外来でのリアルワールド輸液を再考する:Non criticalとCriticalに場合分け~
柴﨑 俊一
-
記事
3Rで整理する 輸液の基本の「き」 ~Resuscitation:Criticalな患者の輸液総論:“ROSD” 敗血症を例に~
- 研修医
- 専攻医・専門医
3Rで整理する 輸液の基本の「き」 ~Resuscitation:Criticalな患者の輸液総論:“ROSD” 敗血症を例に~
柴﨑 俊一
-
記事

3Rで整理する 輸液の基本の「き」 ~Resuscitation:敗血症のOptimization phaseをどう乗り切るか?~特に侵襲的モニタリングなし~
- 研修医
- 専攻医・専門医
3Rで整理する 輸液の基本の「き」 ~Resuscitation:敗血症のOptimization phaseをどう乗り切るか?~特に侵襲的モニタリングなし~
柴﨑 俊一
関連する記事・インタビュー
-
記事

3Rで整理する 輸液の基本の「き」 ~Redistribution:あえて代謝性アルカローシスを例に考える~
- 研修医
- 専攻医・専門医
3Rで整理する 輸液の基本の「き」 ~Redistribution:あえて代謝性アルカローシスを例に考える~
柴﨑 俊一
-
記事

3Rで整理する 輸液の基本の「き」 ~Redistribution:低K血症の補正~
- 研修医
- 専攻医・専門医
3Rで整理する 輸液の基本の「き」 ~Redistribution:低K血症の補正~
柴﨑 俊一
-
記事

3Rで整理する 輸液の基本の「き」 ~Redistribution:低Na血症の補正を超深掘り~
- 研修医
- 専攻医・専門医
3Rで整理する 輸液の基本の「き」 ~Redistribution:低Na血症の補正を超深掘り~
柴﨑 俊一
-
記事

3Rで整理する 輸液の基本の「き」 ~Resuscitation:敗血症のStabilization期やDe-escalation期をどうするか?~
- 研修医
- 専攻医・専門医
3Rで整理する 輸液の基本の「き」 ~Resuscitation:敗血症のStabilization期やDe-escalation期をどうするか?~
柴﨑 俊一
人気記事ランキング
-

書評『循環器のトビラ 循環器には興味がある でもちょっと苦手 そんな皆さんようこそ』
- 新刊
- 研修医
- 医書マニア
書評『循環器のトビラ 循環器には興味がある でもちょっと苦手 そんな皆さんようこそ』
三谷 雄己【踊る救急医】
-

臨床・教育・創薬――医師だから描けるキャリアの循環
- ワークスタイル
- 就職・転職
- 病院以外で働く
臨床・教育・創薬――医師だから描けるキャリアの循環
株式会社ヒューマンダイナミックス、
-

著者が語る☆書籍紹介 『がっこうとコロナ』
- 新刊
- 研修医
- 医書マニア
著者が語る☆書籍紹介 『がっこうとコロナ』
松下隼司、オクダサトシ
-

それ、ChatGPTが代わりにやります! “02 論文を「アップロード」するだけでプレゼン完成
- Doctor’s Magazine
それ、ChatGPTが代わりにやります! “02 論文を「アップロード」するだけでプレゼン完成
白石 達也
-

医師が後回しにしがちな、もったいない控除枠3選!
- ライフスタイル
- 専攻医・専門医
- お金
医師が後回しにしがちな、もったいない控除枠3選!
-

書評『終末期ディスカッション 外来から急性期医療まで 現場でともに考える』
- 新刊
- 研修医
- 医書マニア
書評『終末期ディスカッション 外来から急性期医療まで 現場でともに考える』
三谷 雄己【踊る救急医】
-
医療のリアルを届ける──しろひげコンシェルジュ【3】
- ワークスタイル
- ライフスタイル
- 就職・転職
医療のリアルを届ける──しろひげコンシェルジュ【3】
しろひげコンシェルジュ
-

著者が語る☆書籍紹介 『最新科学が覆す 体にいいのはどっち?』
- 新刊
- 研修医
- 医書マニア
著者が語る☆書籍紹介 『最新科学が覆す 体にいいのはどっち?』
山田 悠史
-
会員限定

ちょっと話そう、研修医のホンネ。Vol. 5 進路の迷いとこれからの目標 ―進路・出会い・そして未来への一歩―
- 研修医
- ワークスタイル
- ライフスタイル
ちょっと話そう、研修医のホンネ。Vol. 5 進路の迷いとこれからの目標 ―進路・出会い・そして未来への一歩―
-

著者が語る☆書籍紹介 『臨床医のためのライフハック(「診療・研究・教育」がガラッと変わる時間術)』
- 新刊
- 研修医
- 医書マニア
著者が語る☆書籍紹介 『臨床医のためのライフハック(「診療・研究・教育」がガラッと変わる時間術)』
中島 啓
